hachi
このサイトは商品プロモーション(Amazonアソシエイト含む)を掲載しています。
Profile
・106回薬剤師国家試験現役合格⇒76%(264/345)
・国試模試で化学全国23位
・Xフォロワー1,500人
・Threadsフォロワー18人
・ブログ約200記事
・国試の年に日本化粧品1級、アロマテラピー検定1級取得
プロフィールを読む
- 構造が覚えられない根本的な原因
- アミノ酸を覚える意義
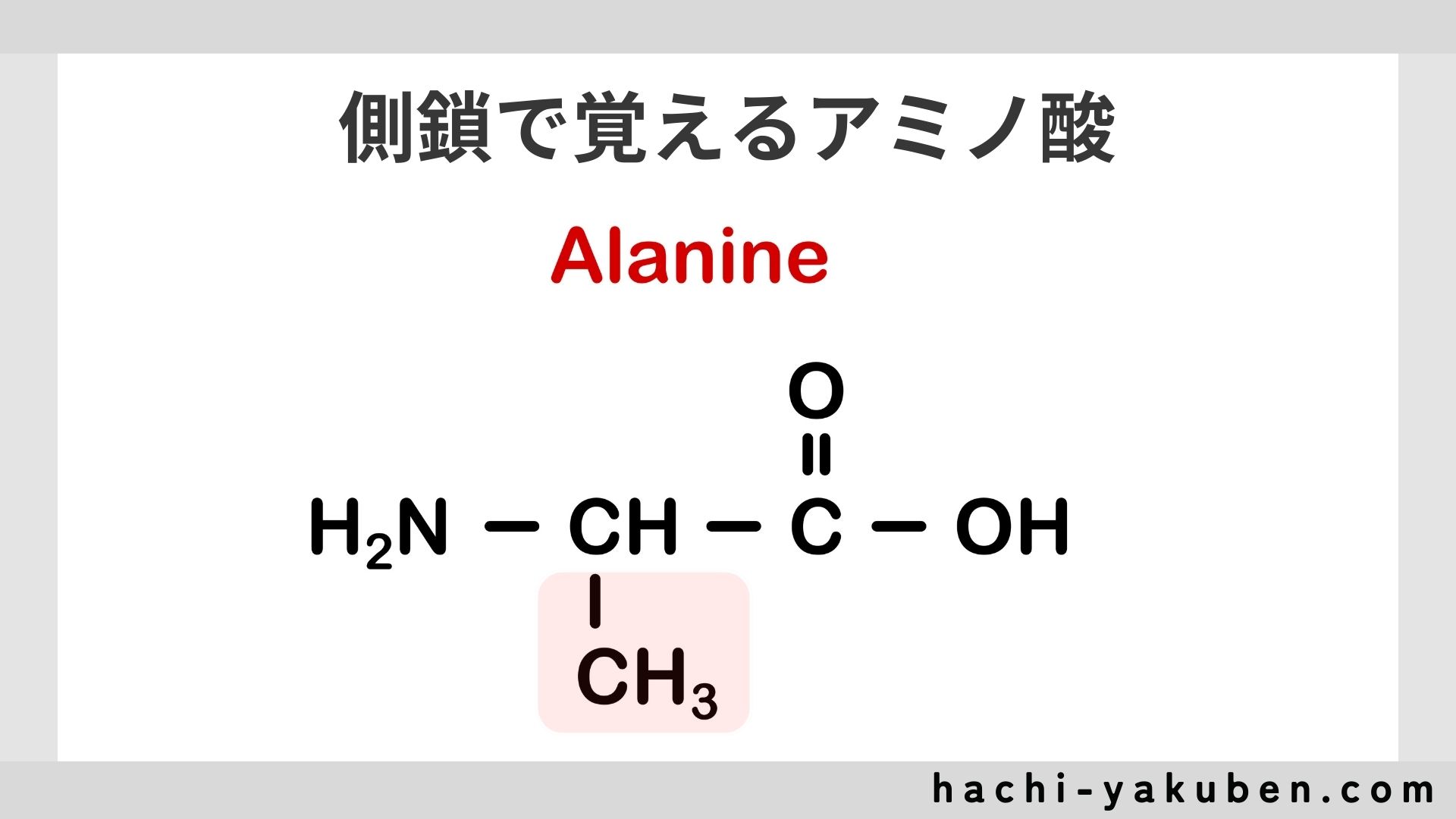
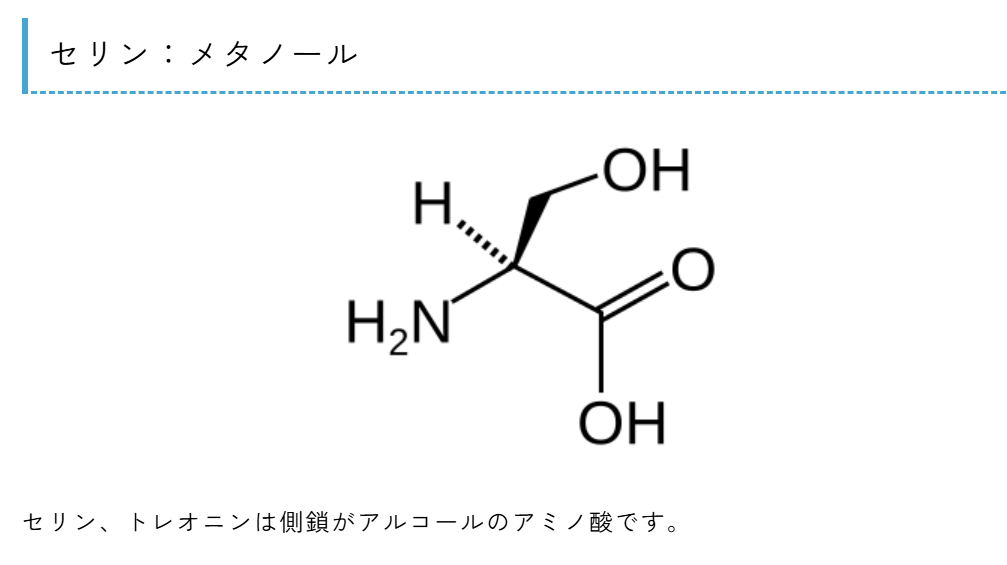
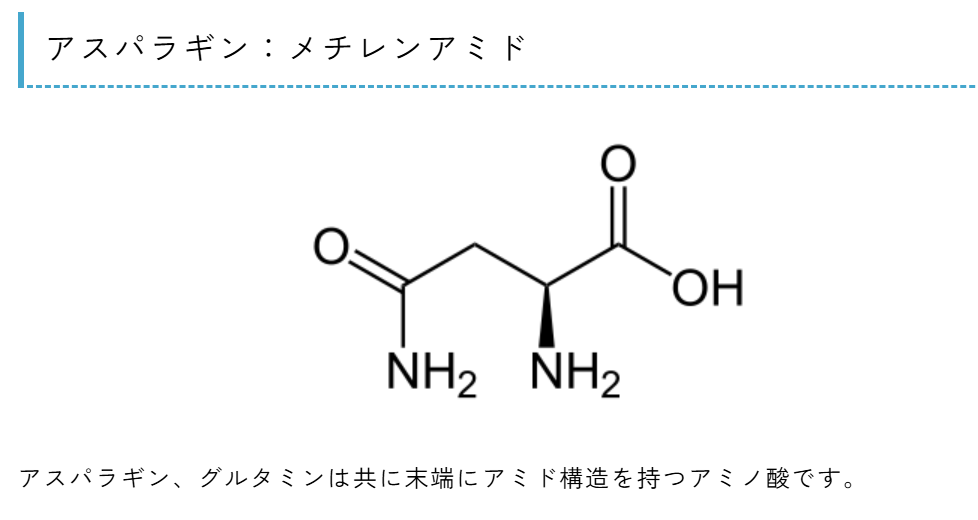
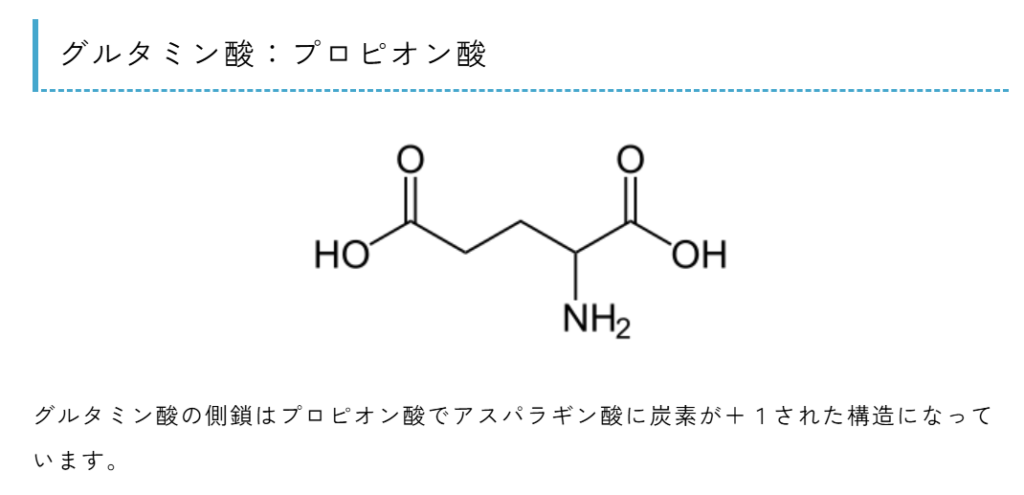
- 側鎖で覚えるアミノ酸(20種類)
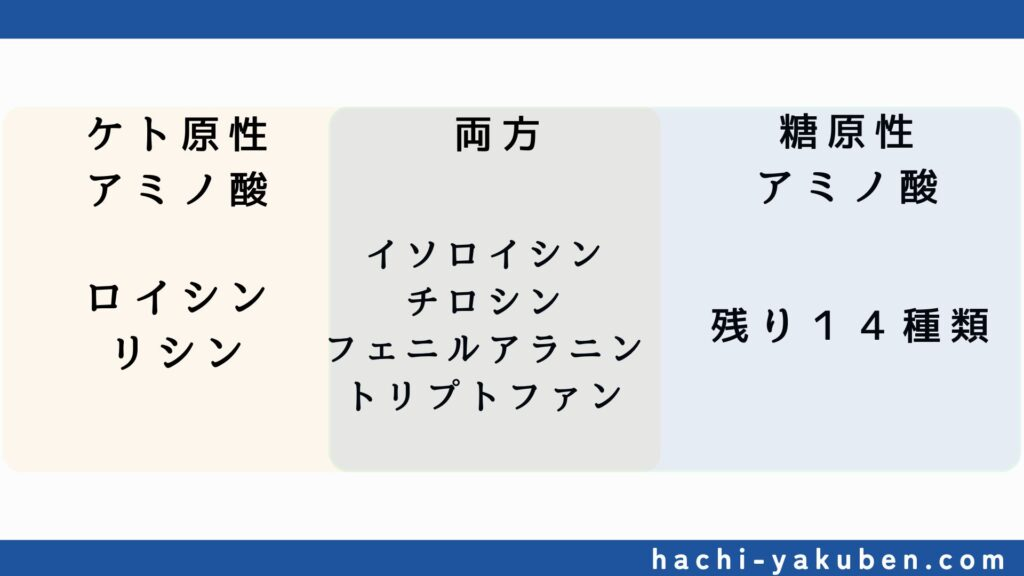
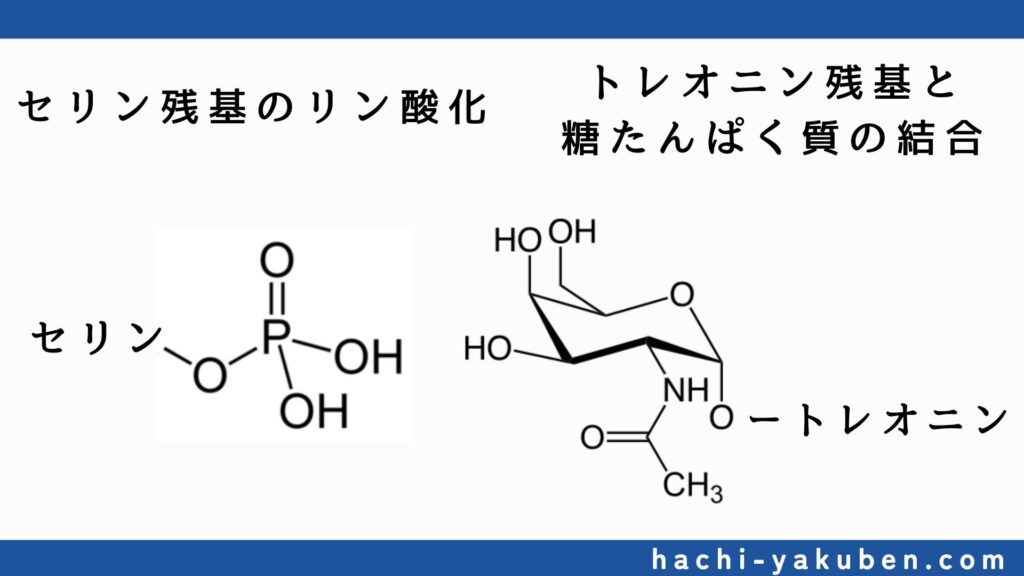
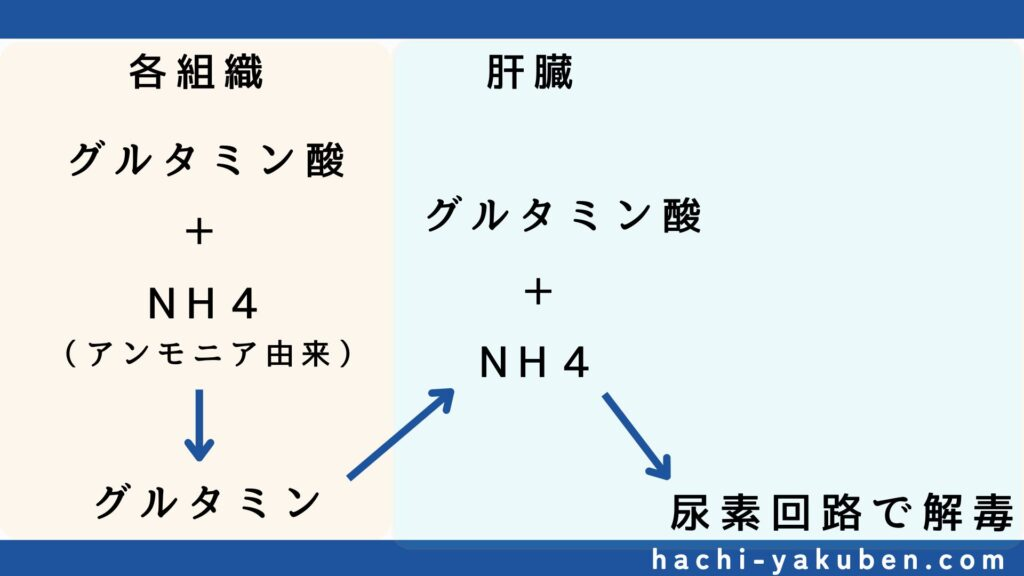
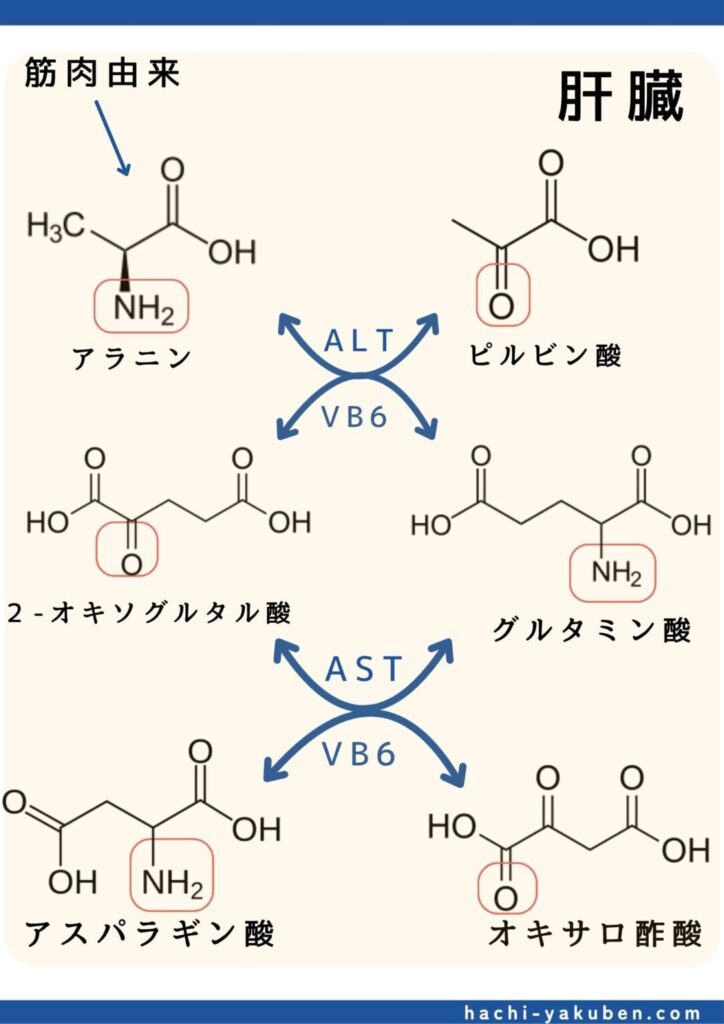
- 各アミノ酸の関連事項
- 関連国試問題
記事の最後
↓
「アミノ酸の覚え方一覧」を用意してるので
ダウンロードして活用して下さい。
(再配布禁止・転載厳禁)
有料記事の価格について
記事内容は日々アップデートしているので
今が一番安い価格になっています。
完成に近づくにつれて値上げしていくので今購入するのが最もお得になっています。
ここから先は限定公開です
すでに購入済みの方はこちら
ABOUT ME

・106回薬剤師国家試験現役合格⇒76%(264/345)
・国試模試で化学全国23位
・Xフォロワー1,500人
・Threadsフォロワー18人
・ブログ約200記事
・国試の年に日本化粧品1級、アロマテラピー検定1級取得